Fallece de COVID-19 una persona de 45 años de edad
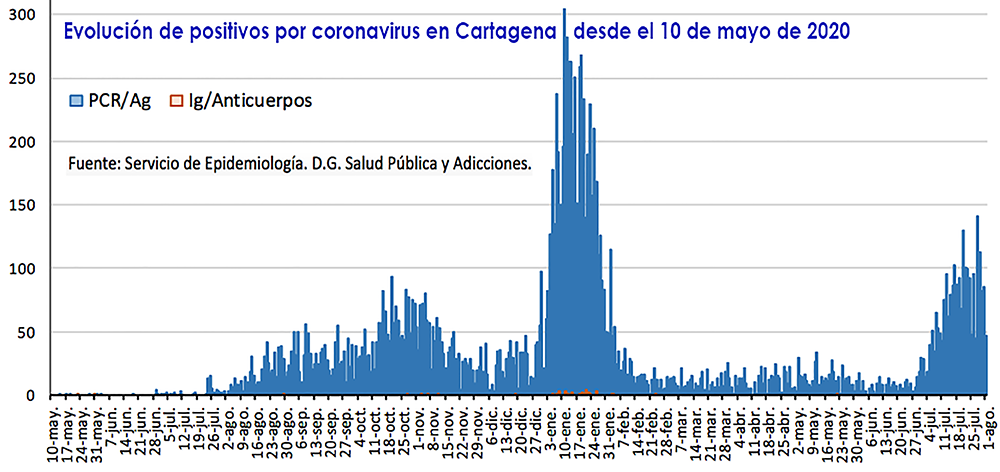 Han sido cuatro las víctimas mortales en la Región de Murcia en el último día a causa del coronavirus. Los contagios totales fueron 507 (58 en Cartagena) y la cifra de enfermos activos vuelve a superar los cinco mil. Por contra, se produce un ligero descenso de hospitalizados.
Han sido cuatro las víctimas mortales en la Región de Murcia en el último día a causa del coronavirus. Los contagios totales fueron 507 (58 en Cartagena) y la cifra de enfermos activos vuelve a superar los cinco mil. Por contra, se produce un ligero descenso de hospitalizados.
🏥 El 45% de la población regional de entre 12 y 19 años ya ha recibido una dosis de la vacuna
🏥 Autorizado el primer ensayo clínico de una vacuna española frente al virus, que, si todo va bien, podría estar funcionando en la sociedad a principios de 2022. Otra empresa también ha pedido autorización para ensayar con humanos
Informe de Epidemiología de la Región de Murcia a fecha 11 de agosto: pinchar aquí
La Región registró ayer cuatro fallecimientos a causa del coronavirus. Se trata de dos hombres y dos mujeres de 89, 45, 80 y 88 de las áreas II, III, VI y VIII.
De los 507 nuevos casos, 140 corresponden al municipio de Murcia, 65 a Lorca, 58 a Cartagena, 37 a Molina de Segura, 15 a Mazarrón, 13 a Alcantarilla, 12 a Ceutí, 12 a San Pedro del Pinatar, 12 a Torre Pacheco, 12 a Totana, 11 a Archena, 10 a Alhama de Murcia, 9 a Águilas, 9 a San Javier, 8 a Caravaca de la Cruz, 7 a Las Torres de Cotillas, 6 a Cehegín, 6 a Fortuna y 5 a Los Alcázares, Lorquí y La Unión. El resto están repartidos por los demás municipios.

CONSEJO INTERTERRITORIAL DEL SISTEMA NACIONAL DE SALUD
Esta mañana, el consejero de Salud, Juan José Pedreño, ha participado en la reunión del Consejo Interterritorial del Sistema Nacional de Salud donde ha pedido al Ministerio de Sanidad que haga públicos los criterios de distribución de las vacunas e iguale el número de dosis en función de la población a vacunar.
Pedreño manifestó que “es necesario que se haga un reparto equitativo que beneficie a todas las comunidades por igual para alcanzar la inmunidad de grupo que es el objetivo común de todas”.
Asimismo, Pedreño solicitó al Ministerio conocer la planificación definitiva del mes de agosto para seguir aumentando la vacunación de los más jóvenes de cara al próximo curso escolar. El consejero de Salud recordó que “Murcia fue una de las primeras comunidades autónomas en abrir la vacunación a todos los grupos de edad y es una de las autonomías con mayor porcentaje de vacunados de 12 a 19 años con más del 45 por ciento ya vacunados con una dosis”.
El consejero de Salud hizo también un llamamiento a la población que aún no ha solicitado su vacuna para que pida cita ya que “la vacunación y el cumplimiento de las normas están haciendo que se reduzca la incidencia de esta nueva ola, que esta semana ha bajado un 20 por ciento”, explicó.
Además, recordó que todas las medidas de prevención son importantes, pero que hay dos fundamentales: la mascarilla, que se debe seguir usando aun estando inmunizados, y la vacuna “porque evita complicaciones y muertes”.

La Agencia Española de Medicamentos y Productos Sanitarios autoriza el primer ensayo clínico de una vacuna española frente a la COVID-19
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha autorizado el ensayo clínico de la vacuna PHH-1V frente a la COVID-19 de la compañía Hipra. Se trata del primer ensayo en personas de una vacuna desarrollada en España.
Es un ensayo fase I/IIa de escalada de dosis, aleatorizado, controlado y enmascarado (se administra la vacuna de Hipra o una vacuna autorizada enmascaradas, de manera que se impida su identificación tanto por el paciente como por el equipo investigador), que estudiará principalmente la seguridad y la tolerabilidad de esta vacuna, así como su inmunogenicidad y eficacia como objetivos secundarios. Para ello se reclutarán varias decenas de voluntarios de centros hospitalarios que iniciarán, tan pronto como sea posible, el proceso para seleccionar a los voluntarios que cumplan con los criterios de inclusión especificados en su protocolo.
Esta vacuna está basada en dos proteínas recombinantes estructuralmente similares, una correspondiente a la variante alfa y otra correspondiente a la variante beta, que se unen formando una estructura única llamada dímero, y que se acompañan de un adyuvante que incrementa la respuesta inmunológica. Esta combinación es capaz de generar una respuesta inmunológica frente a una de las proteínas del virus SARS-CoV-2, conocida como proteína S (de spike, también llamada proteína espiga en español). Esta plataforma es la misma que se ha utilizado para las vacunas de Novavax y Sanofi/GSK, que ya están en proceso de evaluación para su potencial autorización por parte de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés), pero a diferencia de ellas, expresa proteínas de dos variantes distintas.
En el estudio se dividirá a los voluntarios en grupos (cohortes) y se empezará administrando la dosis más baja a la primera cohorte. Tras la evaluación por parte de un comité independiente de vigilancia de los datos de seguridad de estos participantes, se irán escalando a las dosis siguientes si no se han detectado problemas de seguridad. Esta práctica -habitual en este tipo de ensayos- está orientada a evaluar la dosis óptima de vacuna. Cada participante recibirá 2 inmunizaciones separadas por 21 días.
Durante todo ensayo se llevará a cabo una monitorización estrecha de todos los voluntarios y una identificación de todos los casos de acontecimientos adversos y de infección por SARS-CoV-2 que se vayan produciendo. Esto permitirá llevar a cabo análisis preliminares con datos intermedios que permitan continuar avanzando en la investigación. Sin embargo, será necesario esperar a que el ensayo clínico haya finalizado para poder analizar todos los datos y extraer conclusiones finales.
Estos ensayos clínicos forman parte de los requerimientos que deben llevar a cabo todas las vacunas en investigación para demostrar su calidad, seguridad y eficacia. Solo tras haber sido evaluados y si cumplen con los estándares regulatorios serán autorizadas para su comercialización.
El Ministerio de Sanidad y el Ministerio de Ciencia e Innovación mantienen contacto con otros grupos investigadores que están desarrollando en España vacunas frente a la COVID-19 para apoyarlos en el proceso regulatorio y facilitarles el proceso, a la vez que aseguran que estas vacunas cuentan con todas las garantías de calidad, seguridad y eficacia necesarias para ser, finalmente, autorizadas.
🖌️ Textos remitidos en los que se respetan íntegramente contenido, redacción y ortografía, salvo en el titular y en la entradilla del artículo

